Мы приняли вашу заявку, свяжемся с вами в ближайшее время.

История
Часть товаров из корзины будет перемещена в статус отложенных и не сможет быть оформлена для заказа, если вы продолжите работу в данном регионе
История

История
История
Первые работы, которые научная группа В.М. Говоруна провела в том же направлении, начаты с интервалом около трех лет после группы Серрано – на другом объекте, с опорой на силы сначала одной, а потом двух лабораторий в Институте физико-химической медицины. Но зато в руках исследователей были сосредоточены все методы, которые были доступны и группе Серрано, только в разных местах.
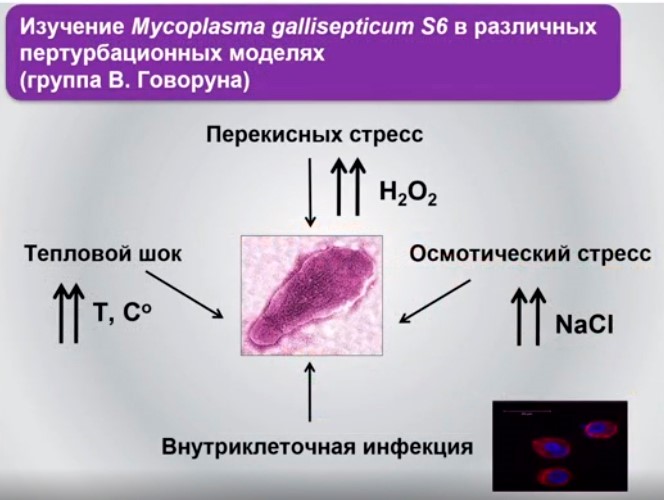
Цель была одна — найти какие-то принципиально новые механизмы и просто хотя бы разобраться в каталогизации старых механизмов регуляции. А также объяснить довольно простую с точки зрения химиков задачу: как 225 метаболитов 225-230-ти биохимических реакций, какие-то эффлюксные процессы, которые приводят к транспорту некоторых простых органических соединений внутри клетки, вместе обусловливают то, что клетка в конце концов начинает делиться, приспосабливается к действию теплового стресса, иммунной системы и так далее. То есть описать весь набор критических регуляторных процессов, без которых клетка не может жить.
Но вот этот переход между репликацией как финальной частью развития жизненного цикла и протеканием химических реакций, о которых молекулярные биологи плохо знают и плохо представляют себе, что вот все гены, транскрипция, синтез белков — это «для чего-то». То есть жизнь – это просто очень хорошо структурированная и синхронизированная химическая динамика. Потому что если представить, что все это можно воспроизвести в пробирке — а это можно воспроизвести в пробирке! – жизнь не получится.
Российские исследователи стартовали примерно с таких же позиций, безусловно отставая в развитии технологий, но их спасало одно очень важное обстоятельство: в отличие от Серрано, В.М. Говорун до этого занимался микоплазмами порядка 30 лет, как Джек Манилофф. Иногда владение объектом важнее, чем методы, используемые для исследования этого объекта.
Было понимание, что у микоплазмы довольно много специфических особенностей, то есть нельзя изучать молекулярную динамику в том состоянии, когда это представляет собой стационарную фазу развития. Поскольку эти организмы очень зависимы от питательной среды, есть много требований к аккуратному созданию так называемых пертурбационных моделей, являющихся хорошим инструментом редукционной эпохи.
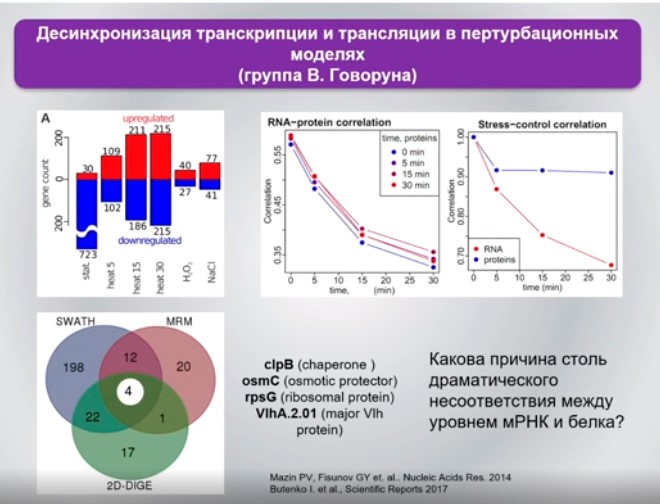
Коэффициент корреляции при развитии хит-шоковой адаптации резко падает, и несмотря на то, что очень много транскриптов в разных пертурбационных моделях меняются «вверх» и «вниз» довольно значительно, количество белков, которое остается неизменным, а не меняется — значительно больше.
В общем случае после тщательных скрупулезных многолетних измерений того, как меняются белки в этой клетке, какова белковая динамика, исследователи обнаружили, что всего лишь четыре белка значимо изменяются на фоне более чем 40% изменения транскриптов.
Они также обнаружили, что на самом деле все еще сложнее, что присутствие транскриптов, которые кодируют одноименные белки, не всегда равняется единице в пересчете на одну клетку. Тут значительно помог drop-in ПЦР.
Вообще вся история системной и потом уже синтетической биологии — это история развития технологий, которые, если их аккуратно использовать и не плодить артефакты, а это требует большой тщательности в подходе — решает дело.
Это был первый вывод, который сильно озадачил исследователей. Как можно регулировать себя и производить те или иные адаптационные процессы, если белковая составляющая не сильно-то и меняется? Среди этих четырех белках, которые здесь представлены — это прежде всего шапероны, белки, которые на самом деле должны меняться, но их очень мало, и не все шапероны, которые присутствуют закодированными в геноме клетки, в данном случае изменены.
Следует отметить различие между понятиями «шум» и «хаос».
Под шумом понимаются некие докритические изменения свойств объекта, которые могут генерировать резонансное изменение какого-либо сигнала в клетках. Показано, что множественные флуктуации каких-то параметров могут приводить к резонансному переходу, например, клетка приобретает какое-то новое свойство, но при этом гибели ее не происходит.
Хаосом в биологическом смысле называется смерть клетки – дестабилизацию всех систем, невозможность репликации – либо клеточный арест, либо просто остановка этой системы навсегда и разрушение клеток в ходе дальнейшего персистирования. Хотя в теории сложных систем процесс перехода (при разрушении) клеток в какие-то структурированные частицы предусмотрен. Когда отмечены хаотические изменения одной микрофазы (поскольку одна модель существования сверхвысоких концентраций в клетке – это межкластерные транзиции), а имеется несколько сверхконденсированных капель, за счет хаотического изменения в одной капле происходит перенос белков или белковых ансамблей в другую каплю или в межкапельное пространство, и там концентрация существенно падает. Но эти процессы очень плохо изучены.
Исследователи сделали довольно много, чтобы разобраться в том, как устроена микоплазма, как она отвечает на те или иные пертурбации, и выяснили, что, в отличие от, например, «традиционной» при обучении во всех вузах кишечной палочки, микоплазма представляет собой «биологическую перфокарту», где предзакодирован, предсуществует ее потенциальный ответ как адаптивная реакция.

Слайд показывает: при наличии транксриптов, которые в штуках квантифицированы относительно клеток меньше единицы, существенную роль играют только те транскрипты, которые присутствуют в клетках, а не предсуществуют, и более того — они еще связаны с рибосомами. И синтез белков, которые необходимы для поддержания так называемого белкового гомеостаза, запускается практически моментально.
Микоплазма – очень медленный организм, в отличие от E. coli: если последняя имеет время репликации 15-20 минут, то у микоплазмы — 1 час. Поэтому для того, чтобы ей не умереть в течение этого адаптивного ответа, она готова всегда быть коммитирована (определенным образом запрограммирована) к тем или иным возможным способам «нападения».
Второе, что увидели исследователи — что этот «шум» может генерироваться своеобразным «проскоком» вследствие адаптации, например, к тепловому стрессу — несовершенной терминацией транскрипции, при которой возникает большое количество аберрантных транскриптов. Они потом элиминируются, и они своей структурой сайта коммитированы к тому, чтобы медленнее связываться с рибосомами.
Это привело к мысли о том, что микоплазма в большей степени борется от наступления внутриклеточного хаоса, чем от наработки тех или иных специфических факторов, функции которых предназначены для адаптации.
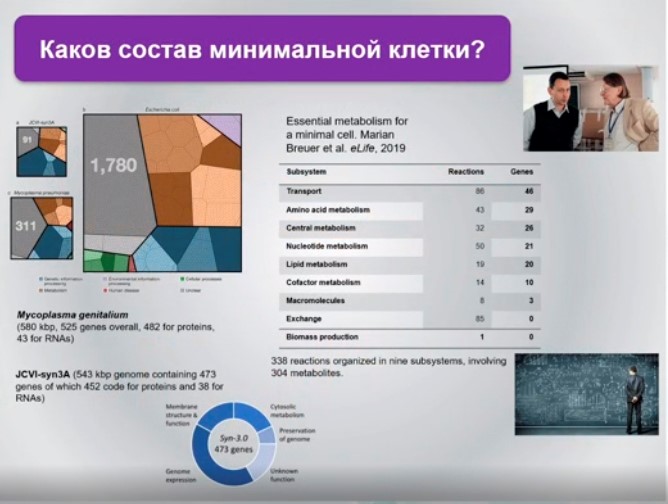
Вопрос, который ставили предшественники российских исследователей, — о том, что такое минимальная клетка — приобрел еще большую актуальность.
Чем глубже становилось погружение в область системной биологии при исследовании метаболических потоков, реакций белков, их модификаций, взаимоотношений этих белков с транксриптами, чем больше исследователи аннотировали возможные транскрипционные факторы (ведь несмотря на то, что эти клетки минимальные, примерно 30-40% геномного контента в них относится к классу unknown), тем больше становилось понимание: довольно трудно определить, что такое минимальный сет, и он вряд ли является универсальным, что очень важно для биологов.
Редукционизм приводит к пониманию, что и в E. coli, и в микоплазме, и в какой-то другой бактерии (геном которой, например, 13 миллионов пар), белковая функция – это некий облачный атлас: белок может обладать почти теми же структурными особенностями, но его функция в данном контексте может либо существенно отличаться (от бытующей в традиционных представлениях), либо отличаться так, что приобретаются новые биохимические свойства.
Возвращаясь к вопросу о том, что такое синтетическая биология, можно сказать: ее определение вытекает из современного понимания сложности даже такого простого организма как клетка микоплазмы.
В минимальной клетке в природе 570049 нуклеотидов, около 340 генов, все остальное отключено либо убрано. Появились синтетические технологии создания таких геномов, но при этом непонятно, как это работает.
Редукционизм сам по себе был очень плодотворной идеей: разбирая клетку на отдельные компоненты, экстрагируя что-то в пробирки, удалось открыть очень много биологических эффектов: цикл Кребса, гликолиз и так далее. Но это все в общем-то реконструкция.
Стало понятно, что синтетическая биология на этом этапе может быть неким новым инструментом при создании тех или иных агрегатоподобных структур – больших олигомерных комплексов. Элиминируя оттуда, например, эффект трансляции или транскрипции, можно попытаться понять, насколько для того или иного комплекса, который существует темпорально и является не очень сильным, можно построить принципиально иную многомерную карту синхронизации процессов. Ведь биология до сих пор в основном изучает сильные взаимодействия – со слабыми она работает очень плохо или вообще не работает.
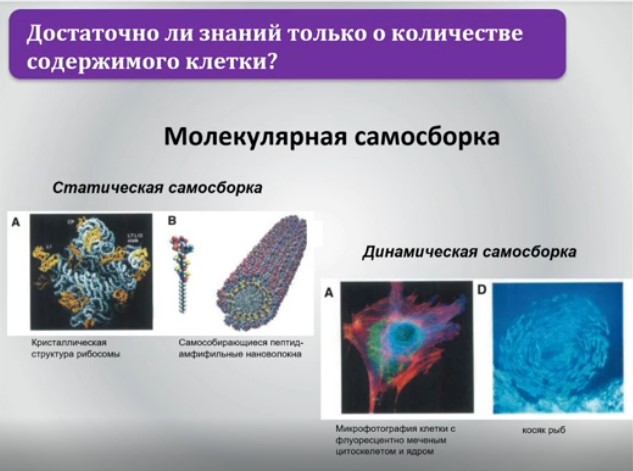
Молекулярная самосборка как в статическом варианте, так и в динамическом хорошо известна биологам: микротрубочки, ансамбли олигомерных ферментов, пируватдекарбоксилаза и другие объекты хорошо изучены. Это явления не сегодняшнего времени, а как раз «родом из» классической биохимии, которую постепенно забывают, потому что она вытесняется генными технологиями. Но самосборка существует – и это некий инструмент того, как предсоздавать некие аналоги больших олигомерных комплексов или чего-то другого, что станет для исследователя новым биохимическим или генно-инженерным стендом. Речь не идет еще о синтетической жизни в целом!
Но все гораздо сложнее.
С помощью личного кабинета Вы сможете:
Сравнение