Мы приняли вашу заявку, свяжемся с вами в ближайшее время.

История
Часть товаров из корзины будет перемещена в статус отложенных и не сможет быть оформлена для заказа, если вы продолжите работу в данном регионе
История

История
История
Терапия химерными T-клетками (CAR-T cell therapy) является новым и перспективным направлением иммунотерапии в лечении онкологических заболеваний. Суть метода заключается в лабораторной генетической модификации выделенных из крови пациента Т-клеток с целью экспрессии химерных антигенных рецепторов (CAR), сочетающих вариабельные участки антиген-распознающих доменов (ScFv) из моноклональных антител с участками доменов T-клеточного рецептора, после чего их размножают и вводят обратно в организм пациента для уничтожения злокачественных клеток-мишеней.
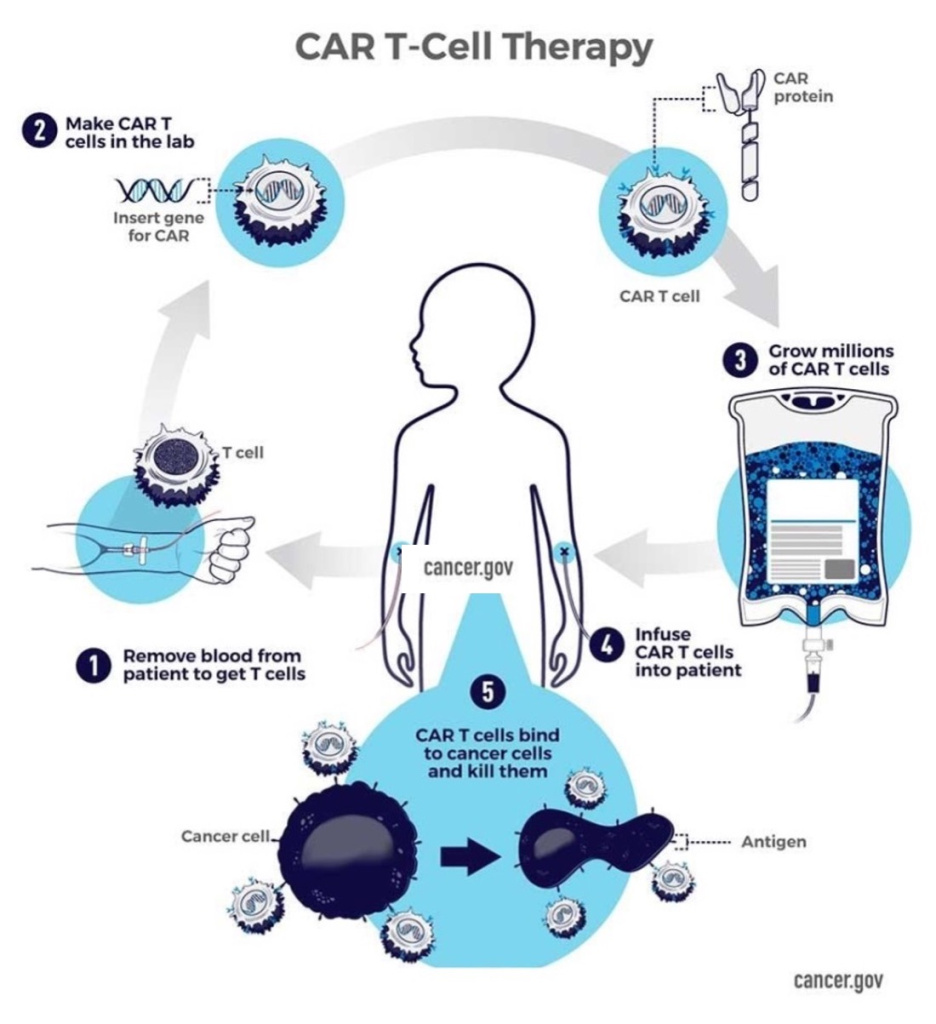
Упрощенная схема CAR-T терапии
(1) Т-клетки пациента удаляются из его крови.
(2) Ген для специального рецептора, так называемый химерный антигенный рецептор (CAR) вводится в Т-клетки в лаборатории. Ген кодирует сконструированный белок CAR, который экспрессируется на поверхности Т-клеток пациента, создавая Т-клетку CAR.
(3) Миллионы Т-клеток CAR выращиваются в лаборатории.
(4) Т-клетки CAR вводятся пациенту путем внутривенной инфузии.
(5) Т-клетки CAR связываются с антигенами раковых клеток и уничтожают их.
(
https://www.cancer.gov/about-cancer/treatment/research/car-t-cells )
На данный момент для создания CAR T-клеток в основном используются метод вирусной трансдукции, с помощью которого достигается конститутивная экспрессия химерных антигенных рецепторов (CAR). Однако у такого подхода есть потенциальные проблемы связанные с безопасностью технологии, например мутации в геноме хозяина, а постоянная экспрессия химерного рецептора – серьезные побочные эффекты, такие как цитокиновый шторм (сильная системная воспалительная реакция) и неврологические расстройства. В связи с этим исследователи стараются использовать невирусные методы доставки для получения CAR T-клеток, которые могут снизить потенциальные риски, связанные с вирусной трансдукцией.
Одной из перспективных технологий невирусной доставки мРНК в клетки являются липидные наночастицы. Липидные наночастицы – это крошечные «пузырьки» из липидов, которые обладают свойством инкапсулировать нуклеиновые кислоты, тем самым способствуя их защите от разрушения и проникновению в целевые клетки. На примере вакцин Pfizer-BioNTech и Moderna, мы можем говорить, что подход к использованию липидных наночастиц для доставки мРНК оказался довольно успешным. Для использования в клинической практике, в том числе и ex vivo для эффективной трансфекции Т-клеток, липидные наночастицы должны соответствовать определенным параметрам. Это должны быть малые (< 200 нм) везикулы с низким индексом полидисперсности (PDI < 0,3) и высокой способностью к инкапсуляции нуклеиновых кислот.
Для получения таких частиц в современных лабораториях используются микрофлюидные системы, которые позволяют точнее контролировать процесс самосборки липидов и мРНК, а также исключить вариации от партии к партии. Одной из таких систем является NanoGenerator от Suzhou Precigenome, которая позволяет получать липидные наночастицы контролируемого размера с высокой гомогенностью и превосходной эффективностью инкапсуляции. С помощью данной системы и стартового набора липидов были получены наночастицы с инкапсулированной мРНК, кодирующей GFP, средний размер которых составил 67 нм, а индекс полидисперсности PDI - 0,106 (Рис. 1). Далее была проведена трансфекция клеточных линий K562 и HepG2, в результате которой были получены предварительные данные, указывающие на ее высокую эффективность (Рис. 2).
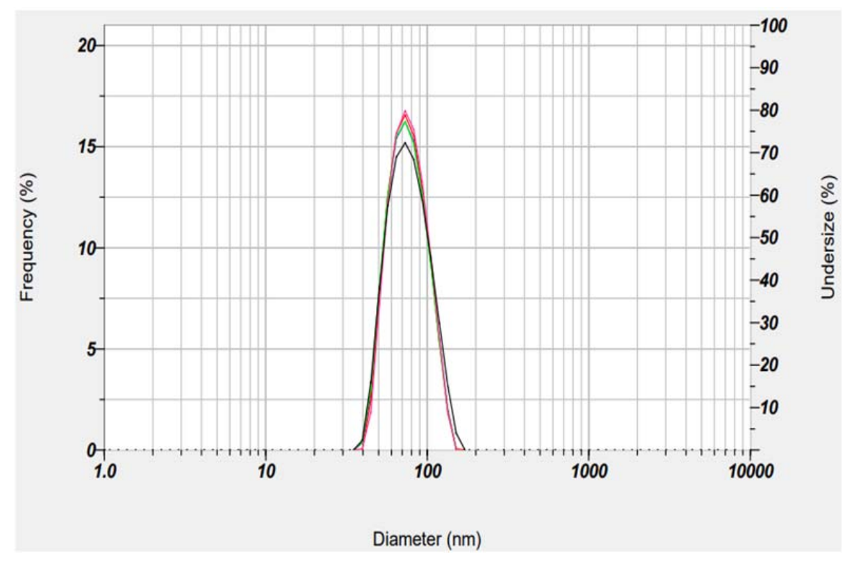
Рисунок 1. мРНК (eGFP)-LNP, синтезированная с помощью NanoGenerator Flex-S.
Средний диаметр 67,3 нм. PDI составляет 0,106. Эффективность инкапсуляции составляет 94,5% (набор для количественного определения РНК Ribo Green).
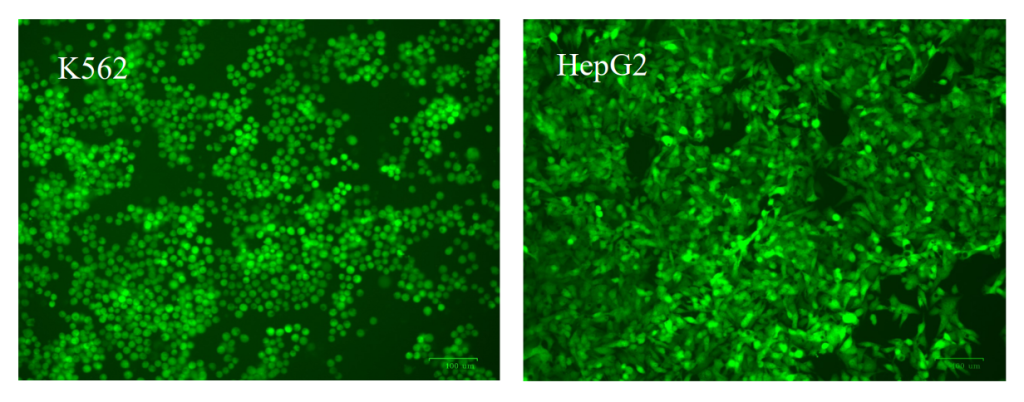
Рисунок 2. Экспрессия GFP в клеточных линиях K562 (слева) и HepG2 (справа) через 48 часов после обработки GFP-LNP, синтезированным с помощью NanoGenerator Flex-S.
Наконец, для количественной оценки эффективности трансфекции первичных Т-клеток был применен метод проточной цитометрии. Анализ показал, что более 98% клеток в результате трансфекции экспрессировали GFP (Рис. 3).
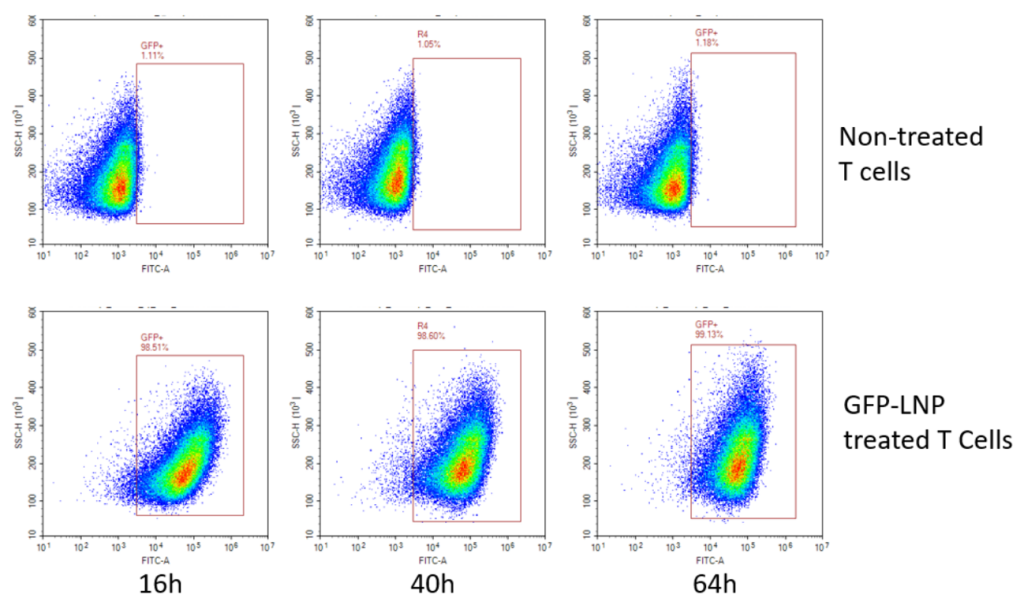
Рисунок 3. GFP(+) положительная популяция контрольных (без лечения) и первичных Т-клеток, обработанных eGFP LNP, через 16, 40 и 64 часа. Для распознавания мертвых клеток использовался краситель 7-AAD. Гейтирование: выделяем область синглетов, исключая дублеты. Затем – популяцию здоровых клеток. Наконец, гейтируем жизнеспособные клетки, неокрашенные красителем 7-AAD, и GFP+ клетки по каналу FITC.
Система NanoGenerator от Suzhou Precigenome является идеальным решением для получения однородных липидных наночастиц для применения в CAR T-клеточной терапии, а благодаря высокой степени контроля и масштабируемости процесса синтеза липидных наночастиц, она может быть применена для решения как исследовательских, так и клинических задач. Кроме того, высокая эффективность инкапсуляции мРНК, обеспечиваемая системой NanoGenerator, может позволить достичь более высоких уровней экспрессии CAR в T-клетках, повысив эффективность терапии CAR T-клетками.

Таким образом, использование системы NanoGenerator для создания липидных наночастиц для доставки мРНК может стать значительным шагом вперед в разработке и применении терапии CAR T-клетками, повысив безопасность, эффективность и доступность CAR T-клеточной терапии, дав новые возможности для лечения онкологических заболеваний.
|
Suzhou Precigenome
Система генерации нанолипосом, NanoGenerator Flex-M, в комплекте |
||||||||||||
|
PG-SYN-FM
|
|
|
|
5 847 958, руб.
|
|
|
|
|||||
|
Система NanoGenerator Flex-M обеспечивает широкий диапазон пропускной способности, от 1 до 12 мл за запуск, что позволит произвести большее количество эмульсии, достаточное для проведения скрининговых исследований. Система Flex-M также имеет функцию разбавления в потоке для мгновенного снижения концентрации веществ, что позволяет влиять стабильность получаемых нанолипосом. Характеристики системы NanoGenerator Flex-M
|
||||||||||||
|
Suzhou Precigenome
Система синтеза наночастиц NanoGenerator Flex-S, в комплекте |
||||||||||||
|
PG-SYN-FS
|
|
|
|
4 548 412, руб.
|
|
|
|
|||||
|
Система NanoGenerator Flex-S предназначена для мелкосерийного синтеза нанолипосом. Диапазон пропускной способности составляет от 0,1 до 2 мл за запуск, что идеально подходит для небольших лабораторий, занимающимися разработками в данной области. При этом, благодаря низкому расходу, система позволяет экономить реагенты (плазмиды, мРНК), используемые при получении эмульсий. Характеристики системы NanoGenerator Flex-S
|
||||||||||||
|
Suzhou Precigenome
Система синтеза наночастиц NanoGenerator Max, производительность 0,2-1 л |
||||||||||||
|
MAX
|
|
|
|
12 892 323, руб.
|
|
|
|
|||||
|
Система NanoGenerator Max представляет собой высокопроизводительную микрофлюидную систему для синтеза наночастиц (LNP, липосомы, PLGA и т. д.) в непрерывном режиме для доклинических исследований и разработок. Производительность системы составляет от 10 мл до 1 л наноэмульсии за цикл. Характеристики системы NanoGenerator Max
|
||||||||||||
|
|
||||||||||||
См. также:
Липосоматоры
Проточные цитометры: анализаторы и сортеры
Системы визуализации биолюминесценции in vivo
С помощью личного кабинета Вы сможете:
Сравнение