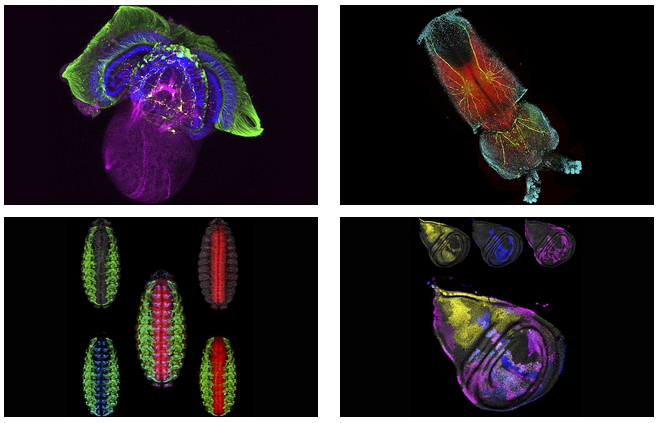
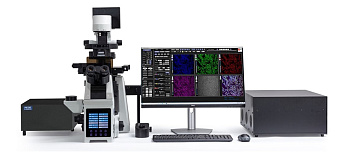
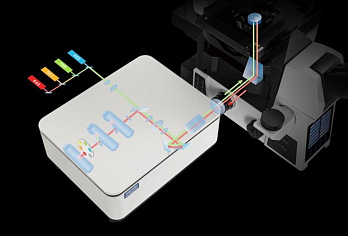
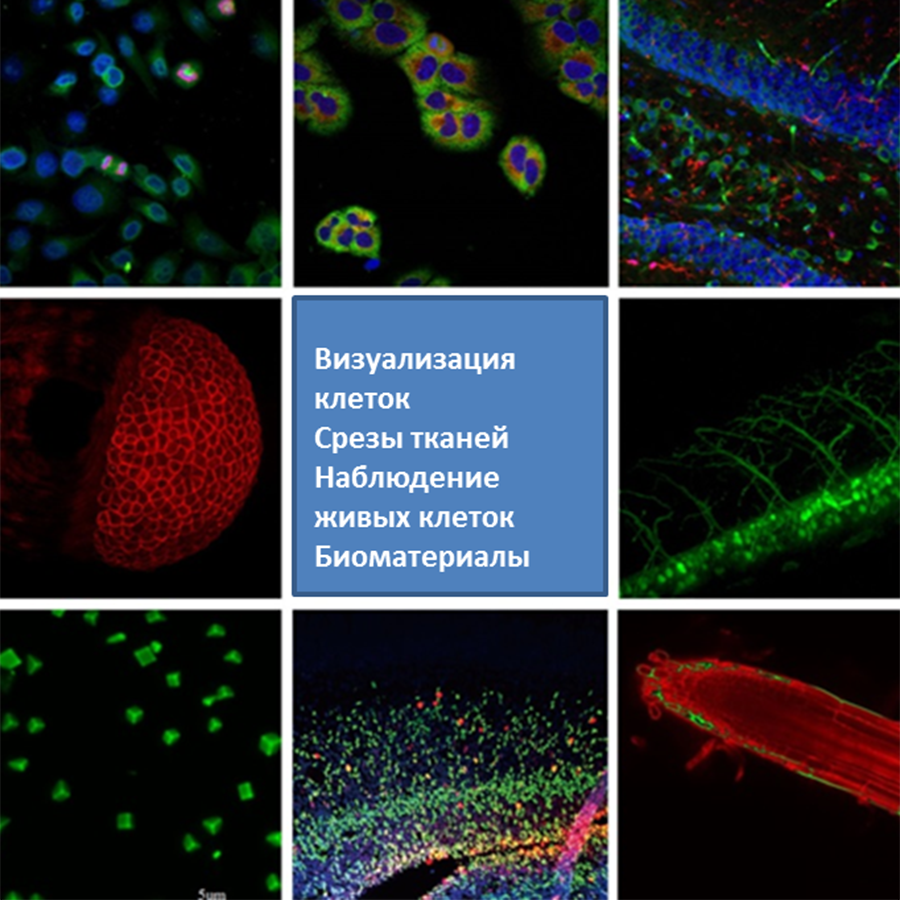
A1R MP – это система получения мультифотонных изображений, оснащенная гальванометрическим сканером высокого разрешения и высокоскоростным резонансным сканером, которые позволяют регистрировать изображения со скоростью от 30 кадров в секунду при разрешении 512 х 512 пикселей до 420 кадров в секунду в режиме полосового сканирования.
Четырехканальные приемники, не требующие десканирования, с более высокой чувствительностью, пониженным темновым током и широким спектральным диапазоном позволяют в реальном времени разделять отклик от близко расположенных зондов для получения точных и высококонтрастных спектральных изображений.
- Резонансный сканер позволяет регистрировать изображения со скоростью до 420 кадров в секунду;
- высокоскоростное формирование изображений глубоких слоев живых образцов с помощью не требующего десканирования NDD-детектора с высокой чувствительностью;
- высокоскоростное и высокоточное разделение за счет использования 4-канального NDD-детектора;
- юстировка мультифотонного лазерного луча одним нажатием кнопки.
Развитие генной инженерии, протеомики, биотехнологии, современной фармацевтики и биомедицины способствовало быстрому внедрению новых методов конфокальной микроскопии, и в настоящее время они широко используются в клеточной биологии.
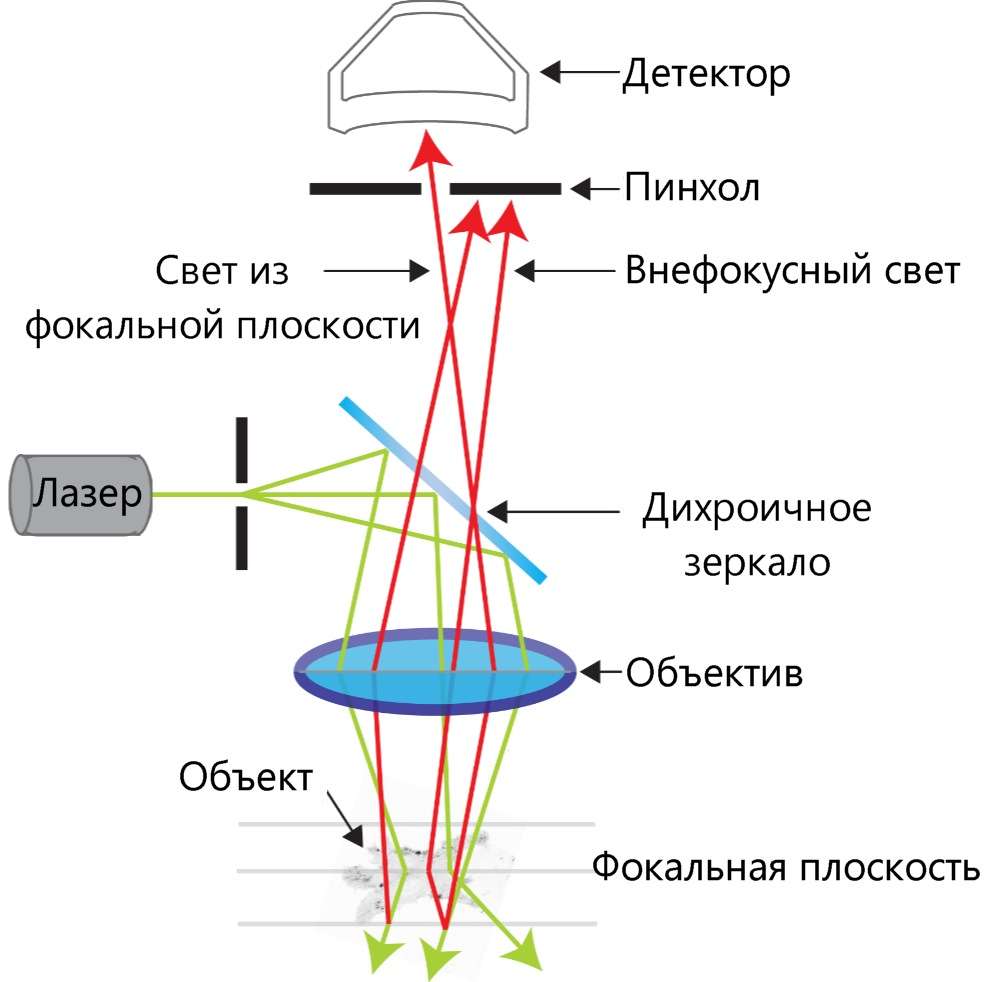
Конфокальную флуоресцентную микроскопию можно рассматривать как разновидность традиционной флуоресцентной микроскопии, которая позволяет исследовать внутреннюю микроструктуру клеток, причем не только фиксированных, но и живых, идентифицировать микроорганизмы, структуры клетки и отдельные молекулы, наблюдать динамические процессы в клетках. Конфокальная флуоресцентная микроскопия в дополнение к этому обеспечила возможность трехмерного субмикронного разрешения объекта и существенно расширила возможность неразрушающего анализа прозрачных образцов. Повышение разрешающей способности достигается благодаря использованию в конфокальных микроскопах лазеров в качестве источников света и конфокальной диафрагмы для фильтрации внефокусной флуоресценции. Преимущество лазеров по сравнению с ртутными или ксеноновыми лампами заключается в монохроматичности и высокой параллельности испускаемого пучка света. Эти свойства лазерного излучения обеспечивают более эффективную работу оптической системы микроскопа, уменьшают число бликов, улучшают точность фокусировки пучка света. На образце лазер освещает не все поле зрения, как в ламповом флуоресцентном микроскопе, а фокусируется в точку. Конечно, при этом лазерный луч возбуждает флуоресценцию как в точке фокуса, так и во всех слоях образца, через которые проходит. И если эта внефокусная флуоресценция, излучаемая слоями, расположенными выше и ниже фокальной плоскости, регистрируется вместе с основным сигналом из фокуса объектива, это ухудшает разрешение оптической системы. Избавиться от внефокусной флуоресценции позволяет конфокальная диафрагма. Изменяя диаметр конфокальной диафрагмы, можно определять толщину оптического слоя вблизи фокуса лазерного луча, поэтому флуоресценция, испускаемая выше и ниже фокуса, оказывается дефокусированной на конфокальной диафрагме и не регистрируется. Благодаря этому конфокальная микроскопия обеспечивает улучшенное разрешение, в первую очередь вдоль оси Z.
Современная конфокальная микроскопия позволяет решать три основные задачи: изучение тонкой структуры клетки, колоколизации (пространственного взаиморасположения) в клетке двух или более веществ, а так же исследование динамических процессов, протекающих в живых клетках.
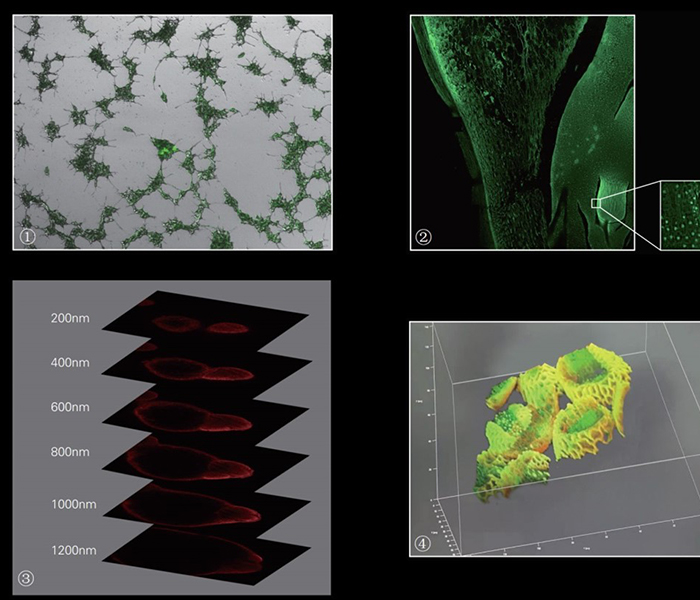
Благодаря улучшенному разрешению, особенно повышенному разрешению по оси Z, и возможности создавать серии «оптических» срезов, конфокальный микроскоп позволяет исследовать тонкую структуру объекта в трехмерном пространстве. Специальные программы позволяют создать из серии оптических срезов объемное изображение объекта (3D) и как бы рассматривать его под разными углами зрения, что может дать ценную информацию о форме клеток, цитоскелете, структуре ядра, хромосомах и даже локализации в них отдельных генов, а так же о взаиморасположении этих элементов.
Использование мультиспектрального (с несколькими флуорохромами) режима работы лазерного сканирующего конфокального микроскопа позволяет исследовать колоколизацию (пространственное взаиморасположение) в клетке двух или более разных веществ, например, белков, помеченных разными флуоресцентными красителями. Исследуя такие препараты в обычном флуоресцентном микроскопе, нельзя с уверенностью утверждать, находятся эти вещества рядом или одно под другим. С помощью метода оптических срезов и дальнейшей 3D-реконструкции объекта можно воссоздать объемное распределение веществ. Мультиспектральный режим так же позволяет проводить на конфокальном микроскопе исследования методом FISH.
Возможность получать временные серии изображений с высоким пространственным разрешением позволяет исследовать изменения, происходящие в клетках и их структурах во времени (4D реконструкция). Кроме того, благодаря наличию лазеров и системы сканирования можно осуществлять не только регистрацию временных изменений, но и осуществлять воздействие на клеточные структуры лазерным излучением с одновременным наблюдением протекающих процессов.
Методы лазерной сканирующей конфокальной микроскопии получили широкое распространение в фундаментальных науках, а также все шире применяются в практических исследованиях и диагностической медицине.
Методы конфокальной микроскопии позволяют выявить способность веществ накапливаться в цитоплазме, ядре или других структурах клетки, зарегистрировать образование метаболитов, измерить кинетику накопления и метаболизма веществ в клетке, скорость выведения веществ из клетки, сравнить интенсивность метаболизма в различных клеточных линиях и в различных условиях. Эти методы все шире применяются в исследованиях механизмов действия как канцерогенов, так и лекарственных препаратов и противоопухолевых соединений, позволяют рассчитывать их эффективные концентрации.
Анализ интенсивности и формы спектров собственной флуоресценции позволяет распознавать нормальные и воспаленные клетки, и такой метод, в частности, предложен в качестве нового способа ранней диагностики шейки матки.
Подобрав комбинацию фильтров для нескольких типов собственной флуоресценции, возможно без проведения гистохимического окрашивания и трудоемкого получения и исследования множества срезов различать злокачественные и нормальные тканевые структуры в биопсийных пробах лимфоузлов пациентов с лимфоаденопатией различного происхождения.
Методы конфокальной микроскопии широко применяются в эмбриологии и гидробиологии, ботанике, зоологии при изучении структуры гамет, развития и формирования организмов.