Мы приняли вашу заявку, свяжемся с вами в ближайшее время.

История
Часть товаров из корзины будет перемещена в статус отложенных и не сможет быть оформлена для заказа, если вы продолжите работу в данном регионе
История

История
История
Диаэм совместно с компанией Lumiprobe расширяет линейку флуоресцентных красителей для ваших исследований. Доставка данных красителей осуществляется в течение 30 дней!
Флуоресцентные красители (также известные как флуорофоры/реактивные красители) молекулы (небелковые по своей природе) способные поглощать свет с заданной длиной волны и излучат его на другой длине волны. Это явление можно визуализировать и анализировать, используя флуоресцентный микроскоп или гель-док систему.
В результате чего красители часто используют для флуоресцентного мечения различных биомолекул (антител, пептидов, различных белков и т. д.) для таких процессов, как мониторинг доставки лекарств в ткани-мишени, визуализация и другие.
H₂DCFDA представляет собой нефлуоресцирующее производное флуоресцеина — его восстановленную ацетилированную форму. Реагент начинает флуоресцировать только после отщепления ацетильных групп и окисления внутри клетки, превращаясь в 2′,7′-дихлорофлуоресцеин. Он характеризуется флуоресценцией в зеленой области спектра (максимум поглощения при 511 нм, максимум флуоресценции при 533 нм). Реагент подходит для исследования живых клеток и не совместим с фиксацией образцов.
Ацетильные группы в структуре H₂DCFDA повышают его липофильность и улучшают проникающую способность реагента через клеточную мембрану. Попадая внутрь клетки, он деацетилируется клеточными эстеразами, из-за чего приобретает заряд и лучше удерживается внутри клетки. Окисление активными формами кислорода приводит к образованию флуоресцирующего продукта — 2′,7′-дихлорофлуоресцеина и может быть детектировано различными способами, например, с помощью проточного цитометра, планшетного ридера или флуоресцентного микроскопа.
|
Lumiprobe, Россия
Реагент H₂DCFDA (2′,7′-Дихлородигидрофлуоресцеин диацетат), CAS 4091-99-0 |
||||||||||||
|
2247-100mg
|
||||||||||||
|
H₂DCFDA (2′,7′-дихлородигидрофлуоресцеин диацетат) —реагент для изучения продукции активных форм кислорода в живых клетках. Общие свойства реагента H₂DCFDA (2′,7′-дихлородигидрофлуоресцеин диацетат)
Берегите от влаги. Избегайте хранения на свету и излишних циклов заморозки-разморозки стокового раствора. При многократном использовании настоятельно рекомендуется хранить реагент в атмосфере сухого аргона. Спектральные свойства реагента H2DCFDA (2′,7′-дихлородигидрофлуоресцеин диацетат)
Рекомендации по использованию реагента H2DCFDA (2′,7′-дихлородигидрофлуоресцеин диацетат)
|
||||||||||||
|
|
||||||||||||
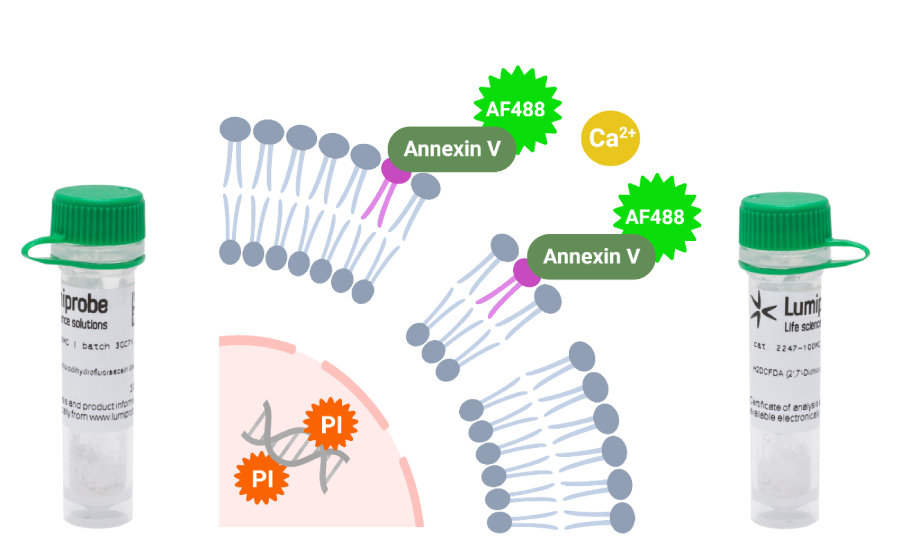
Готовый набор содержит все необходимые реагенты для мечения апоптотических клеток с помощью Аннексина V, конъюгированного с AF488, и PI.
|
Lumiprobe, Россия
Набор для определения апоптотических клеток с помощью аннексина V-AF488 |
||||||||||||
|
21172
|
|
50 тестов
|
хранение -20°C, транспортировка комнатная температура
|
|
18 920, руб.
18 920, руб. RUB
|
|
|
|
||||
|
Набор для определения апоптотических клеток содержит все необходимые реагенты для мечения апоптотических и некротических клеток с помощью аннексина V, конъюгированного с AF488, и йодистого пропидия. AF488 — сульфированный родамин, яркий, фотостабильный и гидрофильный флуорофор. Краситель излучает в зеленом (FITC) канале.
Йодистый пропидий (PI) — непроницаемый через плазматическую мембрану ДНК-краситель, позволяющий различать популяции некротических, апоптотических и здоровых клеток на основе целостности мембраны. После связывания с ДНК краситель излучает в оранжево-красном канале.
Состав набора для определения апоптотических клеток с помощью аннексина V-AF488
Условия транспортировки и хранения
Рекомендуемые концентрации аннексина V-AF488 — от 2 до 5 мкг/мл, в зависимости от исследуемой клеточной культуры. Перед экспериментом необходимо опробовать разные разведения аннексина V-AF488 для определения оптимальной концентрации. Окрашивание с помощью йодистого пропидия — опционально. Этот этап можно пропустить, если в задачах нет необходимости исследовать некроз. Важно! Аннексин V можно использовать в качестве маркера апоптоза только в клетках с интактной плазматической мембраной. При нарушении целостности плазматической мембраны аннексин V может связываться с ФС внутри клетки и давать ложноположительный результат. Применение набора для определения апоптотических клеток с помощью аннексина V-AF488Приготовление растворов1. Растворите содержимое пробирки с лиофилизированным аннексином V-AF488 в 250 мкл деионизованной воды. Важно! Разведенный рекомбинантный белок необходимо хранить защищенным от света при температуре 2-8°C. В растворе конъюгат стабилен в течение месяца. При длительных экспериментах рекомендуется приготовить аликвоты и хранить их при температуре −20°С. Избегать повторного замораживания! 2. Приготовьте необходимый объём 1х буфера для связывания, смешав 1 часть 5х буфера для связывания с 4 частями деионизованной воды. Окрашивание клеток1. Адгезированные клетки аккуратно снимите с поверхности роста подходящим способом. С суспензионными клетками начинайте работу со следующего пункта.2. Промойте клетки один раз охлаждённым PBS (рН7.4) и один раз 1х буфером для связывания. 3. Ресуспензируйте клетки в холодном 1х буфере для связывания. 4. Отберите 100 мкл суспензии клеток (от 1×105 до 1×106 клеток/мл) в микроцентрифужные пробирки объемом 1.5 мл. Для проточной цитометрии необходимо заготовить дополнительные пробирки с соответствующими контролями (см. описание контролей ниже). 5. Добавьте 2-5 мкл раствора аннексина V-AF488 в каждую пробирку, инкубируйте в течение 10-15 мин при комнатной температуре в защищенном от света месте. 6. Без предварительной отмывки добавьте 400 мкл 1x буфера для связывания в каждую пробирку. 7. (Опционально) Добавьте 5 мкл йодистого пропидия в каждую пробирку с клетками. Аккуратно перемешайте содержимое пробирки и инкубируйте в течение 5 мин при комнатной температуре в защищенном от света месте. Важно! Не промывайте клетки от йодистого пропидия. Йодистый пропидий должен оставаться в буфере во время сбора данных. 8. Окрашенные клетки храните при температуре 2-8°C в защищенном от света месте до проведения анализа. Важно! Количественное определение клеток методом проточной цитометрии или флуоресцентной микроскопии необходимо производить в течение 4 ч от начала окрашивания из-за негативного воздействия йодидистого пропидия на жизнеспособность клеток. Проточная цитометрия1. Для цитофлуориметрического анализа апоптоза и некроза клеток с помощью аннексина V-AF488 и йодистого пропидия помимо целевого окрашивания необходимо приготовить контроли: неокрашенные клетки (отрицательный контроль для настройки прибора); клетки, окрашенные только аннексином V-AF488, и клетки, окрашенные только йодистым пропидием (для настройки компенсации). 2. Анализ связывания аннексина V-AF488 проводят с использованием детектора сигнала FITC. 3. Анализ клеток, окрашенных йодистым пропидием, осуществляют с помощью детектора сигнала фикоэритрина. Флуоресцентная микроскопия1. Отберите каплю суспензии с окрашенными клетками и поместите ее на предметное стекло. Накройте клетки покровным стеклом. 2. В качестве альтернативы, адгезированные клетки можно окрашивать непосредственно на покровном стекле. После окрашивания переверните покровное стекло на предметное, так, чтобы клетки находились между предметным и покровным стёклами. 3. (Опционально) Клетки после окрашивания аннексином V, перед визуализацией можно промыть 1х буфером для связывания и зафиксировать в 2% параформальдегиде. Не фиксируйте клетки перед инкубацией с аннексином V-AF488, поскольку любое нарушение клеточной мембраны может вызвать неспецифическое связывание аннексина V с ФС на внутренней поверхности клеточной мембраны. 4. Исследование клеток под флуоресцентным микроскопом осуществляют, используя двойной набор фильтров для FITC и родамина. Результат окрашивания
|
||||||||||||
|
|
||||||||||||
См. также:
Красители флуоресцентные
Планшетные (спектро) фотометры, флуориметры, люминометры автоматические
Проточные цитометры: анализаторы и сортеры
Системы визуализации биолюминесценции in vivo
Вам также может быть интересно:
Антитела и наборы для ИФА для любой области исследования! Обзор применения антител Arigobio
ИФА спектрофотомеры/фотометры, вошеры для планшетов, шейкеры производства Китай и США. На складе!
Проточный цитофлуориметр 7S (ZS-AE7S) для рутинных задач! BioSino, Китай
Флуоресцентные наборы для оценки пролиферации клеток
Исследования in vivo: визуализация, документирование, анализ. Newton, Vilber
С помощью личного кабинета Вы сможете:
Сравнение